Aktivkohle hat sich als äußerst wirkungsvolle Lösung für die Luft- und Gasreinigung etabliert, aber ist Kokosnuss oder Steinkohle die bessere Lösung? Besondere Aufmerksamkeit verdient hier die Verwendung von Aktivkohle, die aus Kokosnussschalen gewonnen wird. Aufgrund ihrer herausragenden Eigenschaften erweist sich diese Variante in bestimmten Anwendungen nämlich als vielversprechende Alternative zu steinkohlebasierten Aktivkohlen.
Wir werfen einen Blick auf die spezifischen Vorteile von Kokosnuss-Aktivkohlen und ihre vielseitigen Einsatzmöglichkeiten in der Gas- und Luftreinigung. Dabei stellen wir exemplarisch Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) als repräsentative Sorten gegenüber.
Kokosnuss oder Steinkohle: Vorteile einer Kokosnuss-Aktivkohle
Aktivkohle ist in der chemischen Industrie nicht mehr wegzudenken. In der Gas- und Luftreinigung reicht ihr Einsatz von der Rückgewinnung wertvoller Rohstoffe über die Entschwefelung von Biogas bis zur Entfernung von organischen Verbindungen. Zusätzlich eröffnen sich mit dem wachsenden Umweltbewusstsein und strengen Emissionsgrenzwerten neue Anwendungsbereiche, insbesondere im Bereich der Entfernung von Schadstoffen aus der Abluft.
Die Auswahl der richtigen Aktivkohle ist nicht immer einfach. Bei einigen Anwendungen in gasförmigen Medien haben Kokosnusskohlen jedoch klare Leistungsvorteile gegenüber Steinkohlen, die sich wie folgt zusammenfassen lassen:
1. Höherer Mikroporenanteil
- Vorteil: Die Menge eines Stoffes, die adsorbiert werden kann, hängt in hohem Maße von der Größe der inneren Oberfläche einer Aktivkohle ab. Der höhere Anteil an Mikroporen von Aktivkohle auf Kokosnussschalenbasis bietet eine größere innere Oberfläche und erhöht vor allem die Adsorptionskapazität für kleinere und flüchtigere Schadstoffe.
- Anwendung: Höhere Adsorptionskapazität bei Vorhandensein von geringen Mengen an Schadstoffen und flüchtigen Substanzen (VOCs).
2. Höhere Härte
Vorteil: Die natürliche Härte der Kokosnussschalen verleiht der Aktivkohle eine widerstandsfähige Struktur, die den Belastungen in bestimmten Gas- und Luftreinigungsanwendungen besser standhält.
Anwendung: Höhere Widerstandsfähigkeit und geringerer Kohleschwund gegenüber aggressiven Medien
3. Geringerer Aschegehalt
Vorteil: Ein geringer Aschegehalt spielt eine entscheidende Rolle bei Anwendungen, in denen organische Verbindungen mit dem Aschegehalt der Aktivkohle stark exotherm reagieren. Die Verwendung von Aktivkohle mit niedrigem Aschegehalt, wie sie in Kokoskohlen zu finden ist, minimiert potentielle Brandrisiken.
Anwendung: Verringerung der Brandgefahr bei Anwesenheit von Ketonen.
4. Nachwachsender Rohstoff
- Vorteil: Der Einsatz von Kokosnussschalen als Rohstoff für Aktivkohle ist nicht nur leistungsstark, sondern auch nachhaltig. Die Verwendung eines nachwachsenden Rohstoffs trägt dazu bei, Umweltauswirkungen zu minimieren und den ökologischen Fußabdruck zu reduzieren.
- Anwendung: Verbesserung der CO2-Bilanz.
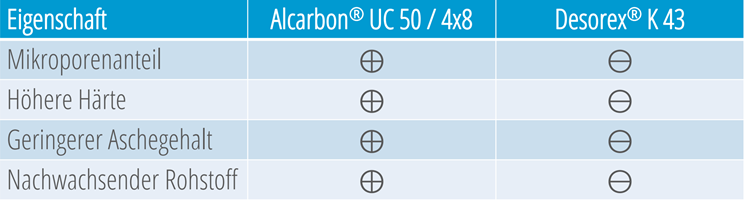 Abbildung 1: Vergleich Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle)
Abbildung 1: Vergleich Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle)
Adsorption an Kokosnuss-Aktivkohle und Steinkohle
Nachfolgende vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) gibt Einblick in die Leistungsfähigkeit kokosnussschalenbasierter Aktivkohle bei der Adsorption bestimmter Stoffe aus einer umgebenden Gasphase.
Zum besseren Verständnis der Adsorptionsisothermen einige Begriffsklärungen:
1. Adsorption:
- Definition: Adsorption beschreibt die Anreicherung eines gasförmigen Stoffes (= Adsorptiv) an der inneren Oberfläche der Aktivkohle (= Adsorbens).
- Beispiel: Wenn Aktivkohle mit einem gasförmigen Medium in Kontakt kommt, etwa mit Luft, das flüchtige organische Verbindungen (VOCs) enthält, führt dies zur Beladung der Aktivkohle mit diesen VOCs, wodurch sich die Konzentration der VOCs in der Luft verringert.
2. Adsorptionskapazität:
- Definition: Die Adsorptionskapazität bezeichnet die Menge eines zu adsorbierenden Stoffes, die von einer bestimmten Menge Aktivkohle aufgenommen werden kann.
- Beispiel: Wenn die Adsorptionskapazität für die Substanz Benzol 20 % beträgt, bedeutet dies, dass die Aktivkohle bis zu 20 % ihres Gewichts an Benzol aufnehmen kann, bevor sie als gesättigt gilt. Mit anderen Worten: 1 kg Aktivkohle kann 200 g Benzol adsorbieren.
3. Adsorptionsisotherme/-gleichgewicht:
- Definition: Die Adsorptionsisotherme ist die grafische Darstellung der Adsorptionskapazität in Abhängigkeit von der Konzentration des Adsorptivs.
- Beispiel: Eine Adsorptionsisotherme für Benzol zeigt, wie die Adsorptionskapazität der Aktivkohle mit steigender Benzolkonzentration in der Luft zunimmt, bis ein Gleichgewichtszustand erreicht ist.
Die Adsorptionsisothermen nachfolgender Beispiele zeigen den Verlauf der Gleichgewichtsbeladung in Abhängigkeit von der Konzentration:
1. Loading (%):
- Definition: Die Gleichgewichtsbeladung bezeichnet die adsorbierbare Menge eines Stoffes bei einer bestimmten Konzentration, bezogen auf das Gesamtgewicht der Aktivkohle, ausgedrückt in Prozent, oberhalb derer keine weitere Beladung stattfindet, da der Anteil der Adsorption dem der Desorption entspricht.
- Beispiel: Wenn die Gleichgewichtsbeladung für Benzol bei 15 % liegt, bedeutet dies, dass 15 % des Gewichts der Aktivkohle an Benzol adsorbiert werden kann, bis ein Gleichgewichtszustand zwischen der Aufnahme (Adsorption) und Abgabe (Desorption) von Benzol erreicht ist.
2. Concentration (g/m3):
- Definition: Die Konzentration entspricht der Masse des zu adsorbierenden Stoffes pro Volumen des umgebenden Mediums, gemessen in Gramm pro Kubikmeter.
- Beispiel: Eine Konzentration von 5 g/m³ Benzol in Luft bedeutet, dass in jedem Kubikmeter Luft 5 Gramm Benzol vorhanden sind.
Anmerkung: Die Adsorptionskapazität oder Gleichgewichtsbeladung einer Aktivkohle für einen bestimmte Substanz ist immer konzentrationsabhängig. Die Menge, die bis zum Erreichen des Gleichgewichtszustandes zwischen Adsorption und Desorption adsorbiert werden kann, nimmt mit steigender Konzentration zu. Dies ist wichtig, um die Leistung und Effizienz von Adsorptionsprozessen zu verstehen.
Kokosnuss-Aktivkohle bei geringer Schadstoffmenge
In zahlreichen Abluft- und Geruchsbehandlungen treten überwiegend niedrige Schadstoffkonzentrationen auf, wie beispielsweise in Industrieparks in der Nähe von Wohngebieten. Unabhängig von der spezifischen Schadstoffsubstanz eignen sich hier Aktivkohlen mit einem hohen Anteil an Mikroporen besser für die Adsorption geringer Schadstoffmengen als offenporige Aktivkohlen. Die Mikroporenstruktur bietet eine erweiterte Oberfläche und somit eine effektivere Interaktion mit den geringfügigen Schadstoffmengen in der Abluft.
Beispiel: Benzol (C₆H₆)
Benzol ist eine flüchtige organische Verbindung (VOC), die bereits bei Raumtemperatur in die Luft verdampft.
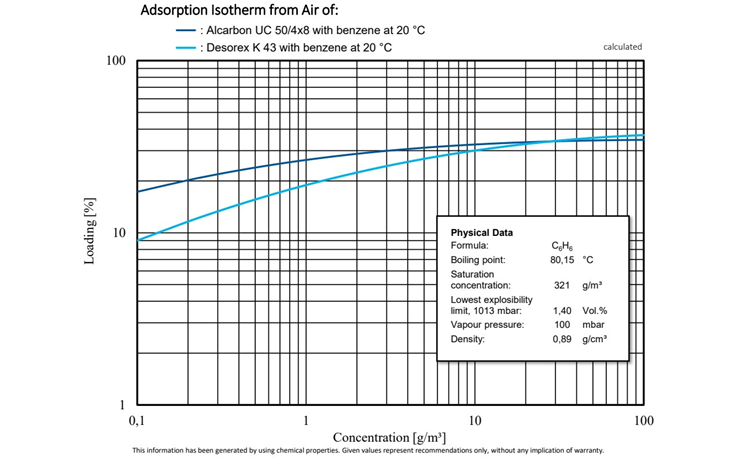 Abbildung 2: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Benzol bei 20 °C.
Abbildung 2: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Benzol bei 20 °C.
Kokosnuss-Aktivkohle bei leichtflüchtigen Verbindungen
Kleine Moleküle mit geringem Molekulargewicht sind schwer adsorbierbar, da sie bestimmte Eigenschaften aufweisen:
-
Volatilität/Flüchtigkeit: Diese Moleküle sind sehr flüchtig, was darauf hinweist, dass sie bei vergleichsweise niedrigen Temperaturen stark verdampfen können.
-
Niedrige Siedepunkte: Sie haben niedrige Siedepunkte, was bedeutet, dass sie bereits bei niedrigen Temperaturen in den gasförmigen Zustand übergehen.
-
Hohe Dampfdrücke: Durch ihre Flüchtigkeit und niedrigen Siedepunkte weisen diese Moleküle hohe Dampfdrücke auf.
Für die Adsorption solcher flüchtigen Verbindungen sind kokosnussschalenbasierte Aktivkohlen mit einem hohen Anteil an Mikroporen besonders geeignet. Typische Beispiele für schwer adsorbierbare Moleküle dieser Art sind:
-
schwefelhaltige organische Verbindungen,
-
halogenierte Kohlenwasserstoffe sowie
-
kurzkettige Kohlenwasserstoffe.
1. Schwefelhaltige organische Verbindungen
Beispiel 1: Kohlenstoffdisulfid (CS₂)
Kohlenstoffdisulfid, auch als Schwefelkohlenstoff bekannt, ist eine flüchtige organische Schwefelverbindung, die in Biogas vorzufinden ist und bei Fäulnisprozessen entsteht.
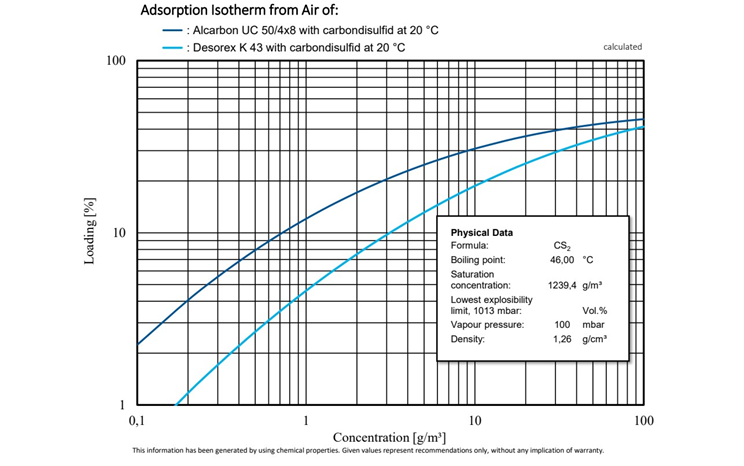 Abbildung 3: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Kohlenstoffdisulfid bei 20 °C.
Abbildung 3: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Kohlenstoffdisulfid bei 20 °C.
Beispiel 2: Dimethylsulfid (C₂H₆S)
Dimethylsulfid (DMS) weist einen sehr niedrigen Siedepunkt von 37 °C auf und tritt vorwiegend im Biogas auf. Ein Problem bei dieser leichtflüchtigen Verbindung ist, dass sie nur physisorptiv adsorbierbar ist. Das bedeutet, dass die Adsorption trotz des niedrigen Siedepunkts nicht auf der chemischen Bindung zwischen Adsorbat und Adsorbens (Chemisorption) beruht, sondern auf physikalischen Wechselwirkungen, den Van-der-Waals-Kräften. Die Mikroporen in der Kokoskohle bieten hier eine ideale Umgebung für die physisorptive Adsorption von DMS.
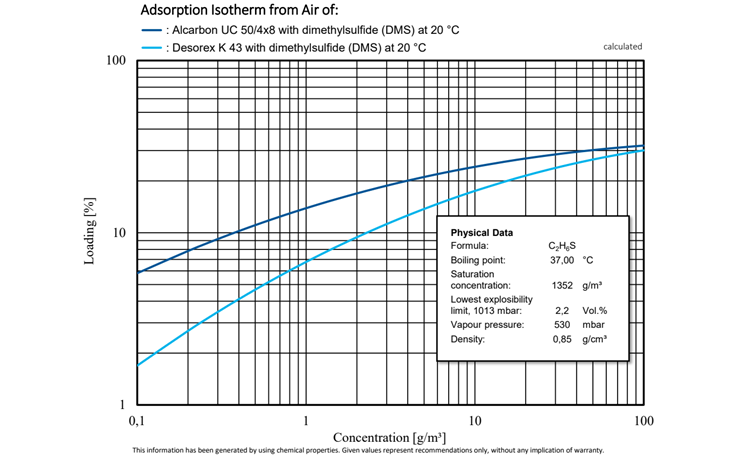 Abbildung 4: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Dimethylsulfid bei 20 °C.
Abbildung 4: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Dimethylsulfid bei 20 °C.
2. Halogenierte Kohlenwasserstoffe
Beispiel 1: Dichlormethan (CH2Cl2)
Dichlormethan (DCM), auch bekannt unter dem Trivialnamen Methylenchlorid, ist eine farblose und nur schwer brennbare Flüssigkeit. Mit einem Siedepunkt von 39,8 °C ist Dichlormethan eine leicht flüchtige Substanz. Aufgrund dieser Eigenschaften wird es häufig als Lösungsmittel für verschiedene Anwendungen verwendet, darunter Harze, Fette, Kunststoffe und Bitumen. Auch hier zeigt kokosnussschalenbasierte Aktivkohle aufgrund der Mikroporenstruktur ihre Überlegenheit gegenüber Steinkohle.
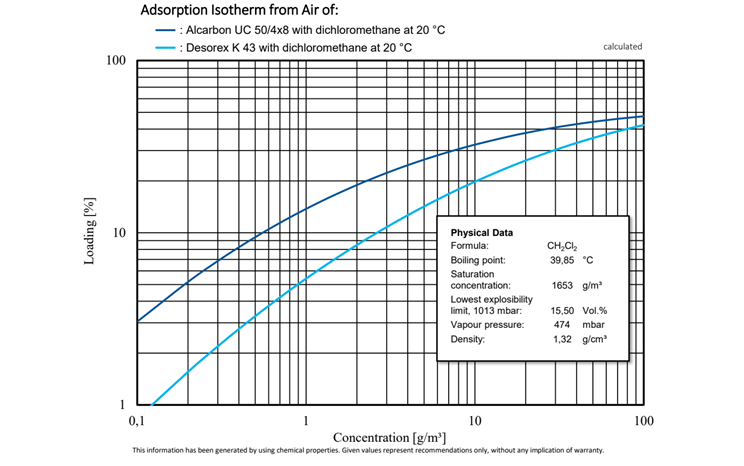 Abbildung 5: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Dichlormethan bei 20 °C.
Abbildung 5: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Dichlormethan bei 20 °C.
Beispiel 2: Trichlormethan (CHCl3)
Trichlormethan, unter dem Trivialnamen Chloroform bekannt, ist eine farblose, nicht entflammbare, flüchtige Flüssigkeit mit einem süßlichen Geruch. Chloroform wird in erster Linie als Lösungsmittel und zur Herstellung von Fluorchlorkohlenwasserstoffen (FCKW) eingesetzt. Bei Normaldruck liegt der Siedepunkt bei 61 °C. Aufgrund seiner flüchtigen Natur verdampft Chloroform auch bei niedrigeren Temperaturen stark. Die kokosnussschalenbasierte Aktivkohle mit ihrer Mikroporenstruktur erweist sich als besonders effektiv bei der Adsorption von Chloroform aus gasförmigen Medien.
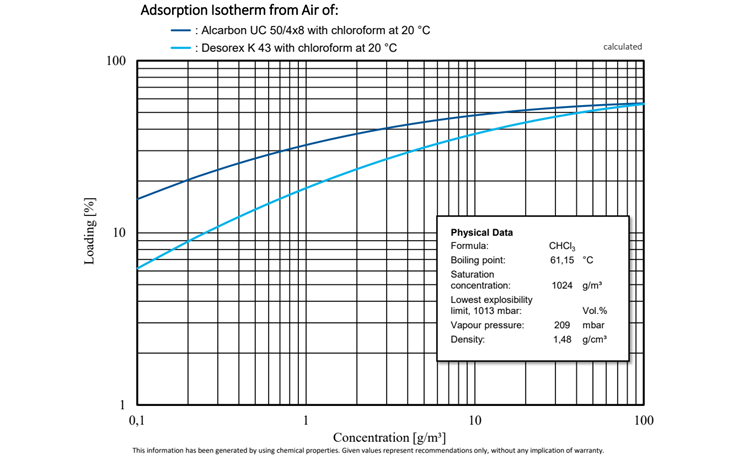 Abbildung 6: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Chloroform bei 20 °C.
Abbildung 6: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Chloroform bei 20 °C.
3. Kurzkettige Kohlenwasserstoffe
Kurzkettige Kohlenwasserstoffe sind eine Gruppe von Kohlenwasserstoffen, deren Moleküle im Vergleich zu ihren langkettigen Pendants geringere Molekulargewichte aufweisen. Es gilt:
Je kurzkettiger ein Kohlenwasserstoff,
-
desto geringer sein Molekulargewicht,
-
desto geringer sein Siedepunkt,
-
desto höher sein Dampfdruck,
- umso schwerer adsorbierbar.
Ein exemplarisches Szenario dieser Zusammenhänge lässt sich anhand von Alkanen (Paraffine) veranschaulichen: Pentan mit fünf Kohlenstoffatomen weist eine geringere Neigung zur Adsorption auf als Hexan mit sechs Kohlenstoffatomen usw. (Pentan < Hexan < Heptan < Oktan < …).
Um eine optimierte Wechselwirkung und Adsorption von kleinen Molekülen, wie sie bei kurzkettigen Kohlenwasserstoffen vorliegen, zu erreichen, hat sich Kokosnuss-Aktivkohle mit ihrem überdurchschnittlich hohen Anteil an Mikroporen bewährt.
Beispiel: Pentan (C5H12)
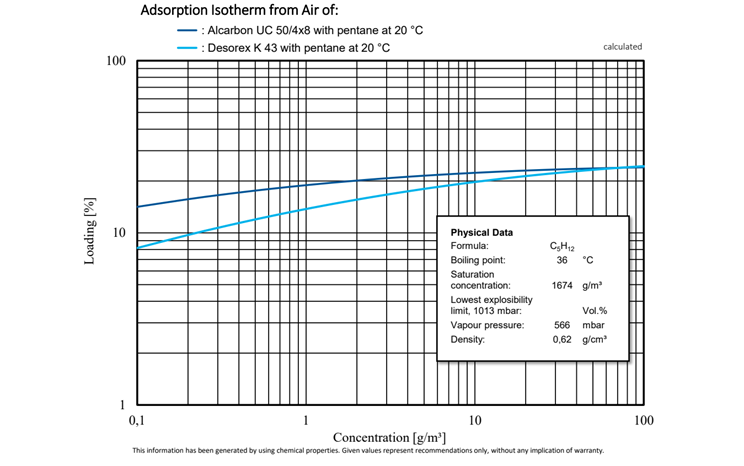 Abbildung 7: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Pentan bei 20 °C.
Abbildung 7: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Pentan bei 20 °C.
Kokosnuss-Aktivkohle bei Anwesenheit von Ketonen
Bei der Adsorption handelt es sich generell um einen exothermen Prozess, d.h. es wird Adsorptionswärme freigesetzt. Ketone enthalten als funktionelle Gruppe eine nicht endständige Carbonylgruppe (C=O), die chemisch reaktionsfähig ist und mit dem Aschegehalt der Aktivkohle zusätzlich stark exotherm reagiert. Es besteht ein höheres Risiko für Wärmeentwicklung und potentiell auch Brandgefahr (Bildung von „Hot Spots“). Daher ist bei Anwesenheit von Ketonen eine Aktivkohle mit niedrigem Aschegehalt, wie Kokoskohle, wichtig.
Prominente Vertreter von Ketonen sind Propanon (Aceton), Butanon (Methylethylketon, MEK), Methylisobutylketon (MIBK) und Cyclohexanon (Azocyclohexan).
Beispiel 1: Propanon (C3H6O)
Propanon, besser bekannt als Aceton, ist ein polares aprotisches Lösungsmittel mit vielfältigen Anwendungen in der chemischen Industrie. Aufgrund seiner Eigenschaften wird Aceton häufig als Ausgangsstoff für zahlreiche Synthesen in der organischen Chemie verwendet.
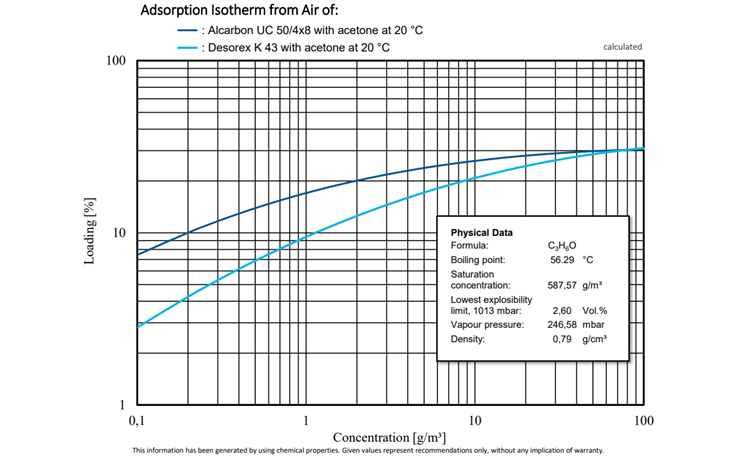 Abbildung 8: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Aceton bei 20 °C.
Abbildung 8: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit Aceton bei 20 °C.
Beispiel 2: Butanon (C4H8O)
Butanon, auch unter dem Trivialnamen Methylethylketon (MEK) geläufig, gehört neben Aceton zu den bedeutendsten industriell genutzten Ketonen. Es findet vor allem Verwendung als Lösungsmittel in verschiedenen industriellen Anwendungen.
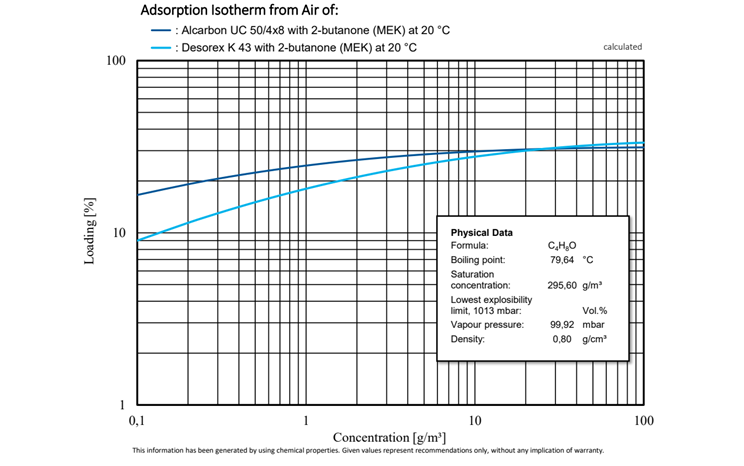
Abbildung 9: Vergleichende Untersuchung der Adsorptionsisothermen von Alcarbon® UC 50/4x8 (Kokosnusskohle) und Desorex® K 43 (Steinkohle) mit 2-Butanon bei 20 °C.
Kokosnuss-Aktivkohle bei aggressiven Medien
Kokosnuss-Aktivkohle zeigt eine hohe Beständigkeit gegenüber einer Vielzahl von aggressiven Chemikalien. Die robuste Struktur verlängert ihre Lebensdauer und gewährleistet eine stabile Leistung, selbst unter anspruchsvollen Bedingungen. Diese Eigenschaften machen sie zu einer bevorzugten Lösung in industriellen Prozessen, in denen eine Aktivkohle mit hoher Härte erforderlich ist.
Beispiel 1: Katalytische Zersetzung
Unter Oxidation der Aktivkohleoberfläche werden einige Substanzen nicht adsorbiert, sondern katalytisch zersetzt. Im Gegensatz zur reinen Adsorption, bei der Moleküle an der inneren Oberfläche der Aktivkohle gebunden werden, führt die katalytische Zersetzung zur chemischen Umwandlung dieser Moleküle an der äußeren Oberfläche. Ein charakteristisches Merkmal dieses Prozesses ist der Kohleschwund oder -verlust, der bei der katalytischen Zersetzung auftritt. Dieser Schwund nimmt mit der Härte der Aktivkohle ab, weshalb Aktivkohlen mit hoher Härte bevorzugt werden.
Ein konkretes Beispiel für die katalytische Zersetzung an Aktivkohle ist der Abbau von Ozonmolekülen. Hierbei zeigt sich, dass die Härte der Kokoskohle eine optimale Umgebung schaffen, die die katalytische Zersetzung von Ozon und anderen Schadstoffen effizient ermöglicht.
Kokosnuss oder Steinkohle: Vergleich der CO2-Bilanzen von Steinkohle- und Kokosnuss-Aktivkohle
Unternehmen richten vermehrt ihr Augenmerk auf den Carbon Footprint von Produkten. Der Vergleich der CO2-Bilanzen zeigt deutlich, dass Aktivkohle aus Kokosnussschalen im Vergleich zu Steinkohleprodukten deutlich besser abschneidet: Die Herstellung von Kokoskohle erzeugt im Vergleich zu Steinkohle nur einen Bruchteil an CO2-Äquivalenten. Betrachtet man den gesamten Lebenszyklus einer Aktivkohle, einschließlich Reaktivierung und Entsorgung, ist die Verwendung von Kokosnusskohle sogar noch umweltfreundlicher.
Wie die Donau Carbon den CO2-Fußabdruck von Aktivkohle berechnet, lesen Sie in unserem Beitrag „Aktivkohle und CO2-Fußabdruck“.
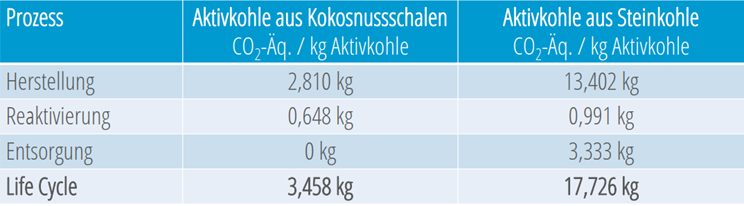
Abbildung 10: Vergleich der CO2 Bilanzen von Aktivkohle aus Kokosnussschalen und Steinkohle. © Donau Carbon
Fazit: Kokosnuss oder Aktivkohle in der Gas- und Lufteinigung
Die Anwendung von Aktivkohle hat sich als äußerst wirkungsvolle Lösung für die Luft- und Gasreinigung etabliert. In bestimmten Anwendungen zeigt die Kokosnuss-Aktivkohle klare Leistungsvorteile gegenüber steinkohlebasierten Varianten.
Der höhere Mikroporenanteil in kokosnussschalenbasierter Aktivkohle bietet eine größere innere Oberfläche und erhöht die Adsorptionskapazität für schwer adsorbierbare Schadstoffe, insbesondere bei geringen Mengen und flüchtigen Substanzen. Der geringe Aschegehalt minimiert das Brandrisiko bei Anwesenheit von Ketonen, während die natürliche Härte der Kokosnuss-Aktivkohle eine höhere Beständigkeit gegenüber aggressiven Medien gewährleistet. Der Vergleich der CO2-Bilanzen unterstreicht zudem die Umweltfreundlichkeit der Kokoskohle im Vergleich zu Steinkohle.
Lesen Sie auch: Auswahl der richtigen Aktivkohle